

尽管非人灵长类是研究人类免疫与疾病的黄金模型,一个根本性矛盾日益凸显:我们对其免疫系统本身的演化“源代码”知之甚少。这种认知缺陷导致两大关键瓶颈:第一,模型可靠性陷阱:由于不清楚物种间免疫差异的遗传根基,直接将模型动物的结果外推至人类存在风险,制约了临床转化研究的精准性。第二,天然解决方案的遗漏:灵长类谱系在千万年演化中淬炼出的、远超人类单一物种的免疫策略库,仍是一座未被系统发掘的“宝库”。因此,系统阐明灵长类免疫多样性的演化动力与遗传机制,是夯实转化医学基础、从演化智慧中寻找人类疾病全新解决方案的迫切需求。
近日,电子游戏app下载安装邵永研究员团队通过整合大规模灵长类基因组数据与表型信息,系统解析了灵长类免疫系统的演化复杂性机制。该研究以“Evolutionary complexity of primate immune system uncovered by the extensive phylogenomic sampling”为题,发表于进化生物学经典期刊─《Genome Biology and Evolution》(https://doi.org/10.1093/gbe/evag087)。电子游戏app下载安装特别研究助理张修平(现任云南师范大学校聘副教授)为该论文的第一作者,邵永研究员为通讯作者。该研究得到国家自然科学基金、云南省基础研究计划等项目的资助。这项研究不仅绘制了免疫基因的模块化演化路径,更取得了两项重要发现:一是揭示了灵长类免疫系统与慢病毒之间可能持续了极为漫长的协同演化史;二是在基因组尺度证实,社会行为的复杂性,而非饮食习性,是驱动灵长类免疫系统多样化的关键演化力量。
研究团队利用长读长基因组测序数据与新型算法(TOGA),成功构建了涵盖广泛灵长类物种抽样的免疫基因图谱。通过解析这些基因在灵长类生命演化树17个关键节点上的选择压力,发现灵长类的免疫基因并非各自为战,而是以“模块”为单位协同演化。成功鉴定了17个演化模块,并根据其选择模式分为三类:1型模块(7个):在全部谱系中均受到强烈的纯化选择,功能上富集于炎症反应,如同免疫系统的“稳定基石”;2型模块(7个):在特定谱系中经历快速演化,驱动了谱系特异的免疫创新;3型模块(3个):在多个谱系中均表现出加速演化,显示出跨谱系的共同适应性演化。其中最引人注目的是3c型模块,该模块的演化压力从灵长类早期祖先开始便持续增强,并在整个人科动物谱系中达到高峰。该模块基因显著富集于对抗HIV-1和流感病毒的响应通路。这一跨越多个关键演化节点的、梯度式的选择压力增强模式,暗示了一场贯穿灵长类演化史大部分历程的、与慢病毒家族的长期‘军备竞赛’。
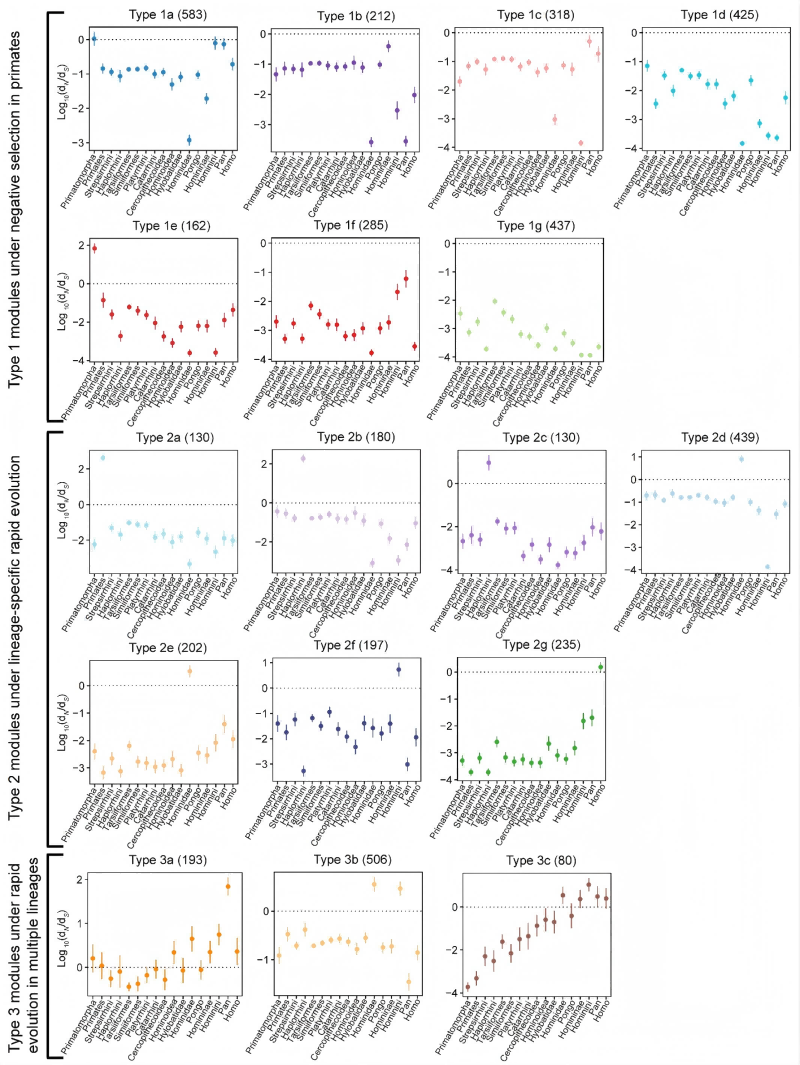
图1:免疫基因演化模块
什么力量塑造了灵长类免疫系统的千差万别?传统观点倾向于强调生态位、群体规模和饮食。本研究通过系统发育最小二乘法分析发现社会结构复杂性和交配系统是解释免疫基因选择压力变异的最显著因素。饮食和群体规模的影响则不具有统计学显著性。
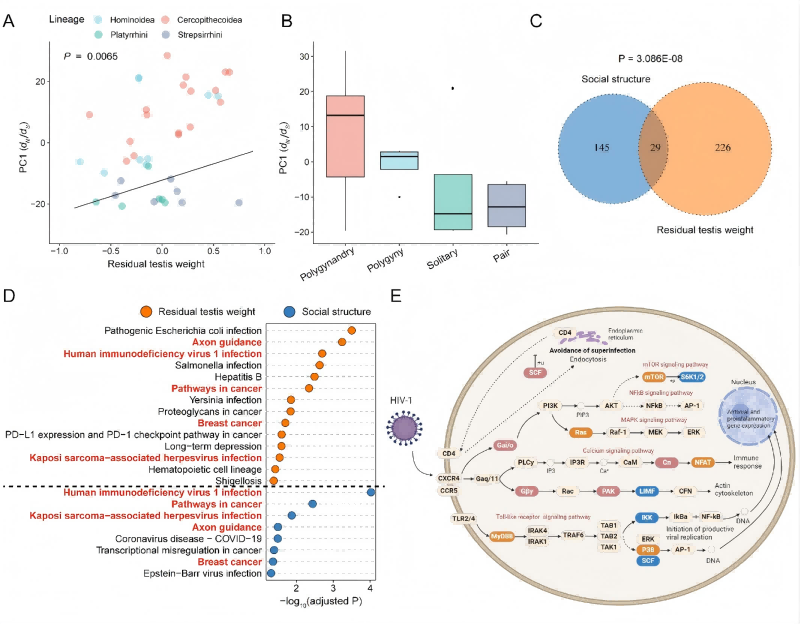
图二:免疫基因演化的社会行为和生态相关性
该研究还对比了人类与近亲实验动物恒河猴的免疫基因演化模式。结果显示,恒河猴谱系中有大量免疫基因经历了独特的快速演化,其中大部分基因在人类谱系中则保持相对保守。这些基因同样富集于重要的免疫相关通路。这一发现本身并不旨在否定动物模型的价值,而是深刻地揭示了演化本身的力量。即使亲缘关系很近的物种,在各自独特的生态和病原体环境中,其免疫系统也会走上不同的适应轨道。这为我们理解生命之树不同分支上‘免疫适应性解决方案’的多样性,提供了一个绝佳的范例。
该项研究的创新性主要体现在在基因组尺度上系统揭示了灵长类免疫基因的模块化演化历史,将社会生态因素与分子演化直接联系起来,并提出了宿主-病原体“军备竞赛”时间轴的新观点。为使用非人灵长类模型的研究提供了至关重要的参考框架和风险警示,该成果不仅深化了对宿主-病原协同演化机制的理解,也为优化非人灵长类疾病模型及人类疾病研究提供了重要理论依据。
